前言
在过去的十年中,T细胞对肿瘤免疫监视的作用得到了广泛研究,而对B细胞的研究相对较少。
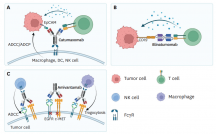
一些研究表明,B细胞的存在和功能可以被视为癌症的一个重要预后因素。此外,浆细胞浸润于肿瘤部位,即使数量很少的细胞也能产生大量的细胞因子和抗体。这些抗体可通过驱动抗体依赖性细胞毒性(ADCC)和吞噬作用、补体激活以及增强树突状细胞的抗原呈递而促进抗肿瘤免疫。
此外,B细胞本身可以向CD4+和CD8+T细胞呈递抗原,从而在肿瘤微环境中形成抗原特异性免疫反应。B细胞也有助于肿瘤相关三级淋巴结构(TLS)的形成,TLS支持肿瘤特异性B细胞的进一步成熟和亚型转换,以及肿瘤特异性T细胞反应的发展。同时,肿瘤浸润性B细胞可能同时发挥促肿瘤和抗肿瘤作用,这取决于肿瘤微环境的组成、存在的B细胞表型及其产生的抗体。B细胞的功能
肿瘤浸润性B细胞
B细胞可集中在肿瘤边缘或形成各种复杂的肿瘤相关免疫聚集体,从无组织的小簇到有结构的TLS。这种结构的细胞组成可能因肿瘤的分期和起源以及其他因素而有很大差异,对各种转移性和原发性肿瘤具有预后价值。特别是,在TLS和肿瘤浸润淋巴细胞群中,T细胞和B细胞之间的抗原特异性相互作用似乎至关重要,而T细胞在肿瘤微环境中的抗肿瘤作用通常取决于与B细胞的合作
肿瘤特异性抗体
肿瘤内抗体首次发现于70年代,1996年,报告了原发性乳腺癌及其转移的病灶中存在IgA1的情况。
多种证据表明,B细胞在肿瘤相关的TLS组织结构中经历克隆增殖、高亲和力抗体的选择和同型转换,最终转化为效应/记忆B细胞和浆细胞。这些浆细胞可能存在于局部并产生高滴度的肿瘤特异性抗体,如乳腺癌、黑色素瘤和高度浆液性卵巢癌。这些抗体可以介导ADCC和CDC的肿瘤细胞杀伤作用,或促进抗体介导的巨噬细胞和粒细胞吞噬肿瘤细胞。
B细胞和抗体的促癌作用
在小鼠模型中的一些研究已经描述了B细胞的促瘤作用。特别是,同基因胸腺瘤、结肠癌和黑色素瘤在B细胞缺陷小鼠中的生长明显慢于野生型小鼠或接受过继转移B细胞的B细胞缺陷小鼠。
包括人类癌症,高水平的B细胞和/或浆细胞浸润到肿瘤中与膀胱癌的侵袭性增加有关,浸润性乳腺癌患者浆细胞和CD138+B细胞浸润率高也与较短的无复发生存率相关。B细胞的促肿瘤作用通常与免疫抑制B细胞亚群(Breg)的存在有关。

局部或全身产生的肿瘤特异性抗体也可能驱动致瘤效应。特别是,已经观察到由肿瘤特异性抗体形成的持久性免疫复合物可能与不利的临床结果有关,这可能是由于调节携带Fc受体的髓系细胞的活性所致。
总之,有足够的证据表明,在某些情况下,肿瘤浸润的B细胞、浆细胞和局部产生的抗体可能产生显著的免疫抑制作用,从而保护肿瘤免受免疫介导的消除。
肿瘤中的抗体亚型
抗体是否具有促肿瘤或抗肿瘤作用的一个重要决定因素是抗体的亚型存在。
人IgG1抗体: 从抗肿瘤细胞毒性反应的角度来看,人IgG1抗体是最重要的,因为这些抗体可以与Fcγ受体(FcγR)结合,触发ADCC和抗体介导的吞噬作用,并介导补体细胞毒性。此外,在树突状细胞和巨噬细胞上表达的FcγR可捕获IgG结合的肿瘤抗原,并将这些抗原衍生肽提供给T细胞。

IgA、IgD和IgE抗体: 值得注意的是,在对TCGA-RNA-seq数据进行的黑色素瘤研究中,高比例的IgA、IgD或IgE与预后不良相关。高比例的IgA亚型也与KRAS突变亚型肺腺癌的阴性预后相关。
一般来说,IgA亚型通常是免疫抑制型B细胞的特征,在这个调节回路中,B细胞促进调节性T细胞(Treg)的增殖,而Treg细胞产生TGF-β,它介导亚型类别转变为IgA。
IgG4抗体:IgG4抗体缺乏抗肿瘤效应器功能,可阻断肿瘤特异性IgG1反应。血清中所有IgG中高比例的IgG4与的不良预后相关,并且肿瘤特异性IgG4抗体已被证明由位于黑色素瘤病灶内的浆细胞原位产生。
在某些癌症类型,IgG4也有积极作用,解释尚不清楚,它可能与IgG4不能形成免疫复合物有关,后者可以刺激慢性炎症和组织重塑过程,并最终诱导免疫抑制性髓系细胞表型。
IgG3抗体:尽管IgG1和IgG3都能触发ADCC、吞噬、补体激活和抗原交叉呈递,但与IgG1相反,IgG3与黑色素瘤患者的存活率呈中性或负相关。一种可能的解释是,尽管IgG3抗体可以与激活的Fc受体相互作用,但有证据表明,这种作用是早期和短暂的,并且IgG3抗体通常具有较低数量的累积超突变和较低的亲和力。

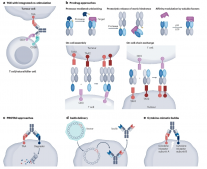
B细胞耗竭疗法
鉴于B细胞的促瘤作用,使用B细胞耗竭的抗CD20抗体,如利妥昔单抗或奥伐单抗作为实体瘤治疗已有研究。然而,临床资料显示,在IL-2治疗转移性肾细胞癌和黑色素瘤后,利妥昔单抗新辅助治疗没有效果。
其他几项临床试验 (NCT01032122和NCT02142335)在没有报告结果的情况下被终止或完成。另一项关于利妥昔单抗治疗实体瘤的试验正在进行中,目的是清除前列腺癌中浸润肿瘤的B细胞(NCT01804712)。
小分子药物如Ibrutinib是抑制B细胞的另一种选择。Ibrutinib以BTK为靶点,BTK是B细胞受体和其他受体(FcγRs、Toll样受体、G蛋白偶联受体)以及B细胞存活、迁移和分化为浆细胞的关键介质。Ibrutinib已作为单一疗法或与其他疗法联合用于治疗各种实体瘤的临床试验中,但B细胞在其中的作用尚不清楚。
总之,已有的研究表明,全B细胞耗竭可能是一种抗肿瘤的干预措施,但其适用范围可能仅限于B细胞起明显负性作用的非常特殊的人群。
肿瘤免疫治疗中的B细胞
考虑到ADCC是抗原特异性抗肿瘤B细胞反应的直接机制之一,刺激NK细胞的药物,例如NKG2A的单克隆抗体monalizumab,有助于对高IgG1浆细胞患者产生更明显的反应。
由于B和T细胞以及B和NK细胞的协同作用,B细胞可能促进PD-1阻断疗法。在非小细胞肺癌的新辅助抗PD-1治疗中,免疫介导的肿瘤清除与TLS的局部形成和浆细胞的存在有关。
抗CTLA-4治疗可显著增加转移癌患者的循环浆细胞数量。这一效应表明,CD4+T细胞介导的抗体亲和力成熟和浆细胞生成的刺激可诱导肿瘤相关B细胞在局部、引流淋巴结以及TLS中产生肿瘤特异性抗体。疫苗接种试验也证明了TLS形成的诱导作用。
小结
综上所述,B细胞不仅仅是肿瘤微环境中的旁观者,而是能够从根本上协调免疫反应的积极参与者。B细胞在一定条件下可以抵御肿瘤,主要是通过产生肿瘤特异性抗体和呈递肿瘤抗原,但某些B细胞亚群和特异性抗体也可以抑制抗肿瘤免疫,促进肿瘤生长。
B细胞在肿瘤环境中的模糊作用决定了免疫治疗方法的不同方向,要么激活阳性B细胞要么抑制阴性B细胞类型。因此,有关B细胞靶向治疗的应用或与其他疗法的结合,应该基于对B细胞谱的深入了解——每个癌症亚型甚至每个患者。
分析、合理解释和使用来自肿瘤相关B细胞的免疫球蛋白谱数据的能力正在成为这个故事的一个重要部分。
参考文献:
1. B cells, plasma cells and antibody repertoires in the tumour microenvironment. Nat Rev Immunol. 2020.