医疗器械方面,FDA有1个通过上市前批准(PMA)途径首次上市的产品。境内公示了8个三类医疗器械进入创新审批绿色通道,批准了3个创新器械上市,境内医疗器械审批集中在体外诊断试剂,共1614项,占44.33%01
美国FDA批准情况
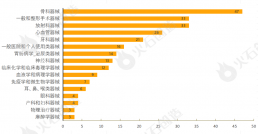
截至2024年4月10日,3月FDA共批准280个510(k)途径的产品,其中一类器械10个,二类器械263个,未分类7个。通过对510(k)上市前通知的器械根据美国医学专业用途进行分类,结果发现,3月产品获批类型最多的为骨科器械、一般和整形手术器械、放射科器械、心血管器械与牙科器械,见图1。

图1 2024年3月通过FDA 510(k)途径获批上市产品类型分布
来源:火石创造产业数据中心
2024年3月有1个通过上市前批准(PMA)途径首次上市的产品。
表1 2024年3月通过PMA首次批准的器械

来源:火石创造产业数据中心
02
境内批准情况
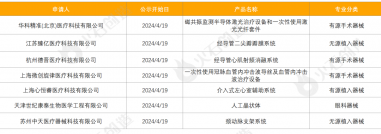
截至2024年4月10日,2024年3月国家局公示了8个三类医疗器械进入创新审批绿色通道,见表2。
表2 2024年3月进入绿色通道的三类创新器械

来源:火石创造产业数据中心
截至2024年4月10日,2024年3月国家局公示了3个三类创新器械获批上市,见表3。
表3 2024年3月获批上市的三类创新器械

来源:火石创造产业数据中心
截至2024年4月10日,2024年3月国家局共批准首次注册三类医疗器械产品325个,其中国产294个,进口31个。各省级药品监管部门3月共批准国产第二类医疗器械注册958个,一类备案医疗器械2269个。统计数据显示,体外诊断试剂数量最多,共1614项,占44.33%,基本上均为国产,为1581项。除体外诊断试剂,批准注册类别数量排前三位的分别为注输、护理和防护器械,口腔科器械和物理治疗器械。表4 2024年2月国产、进口医疗器械批准注册类别数目分布

来源:火石创造产业数据中心
从地域分布上,2024年3月国产二、三类注册产品批件最多的依次为广东省(210件)、江苏省(167件)、河南省(126件)三个区域,见图5。

图2 国产获批器械区域分布
来源:火石创造产业数据中心
—END—
作者 | 火石创造 吴雯雯 审核 | 火石创造 殷 莉
原文标题 : 2024年3月全球医疗器械创新成果进展报告