环状RNA在预测II/III期结肠癌患者复发风险预测中的重要作用
9月2日,中山大学附属肿瘤医院徐瑞华团队发文揭示了,环状RNA在预测II/III期结肠癌患者复发风险中的重要作用,为结肠癌术后的精准治疗提供更好的治疗策略。
该研究团队采用高通量转录组测序技术与LASSO筛选框架的机器学习方法相结合。通过比较20例(复发和未复发各10例)II/III期结肠癌组织标本,分析及鉴定出差异表达的100个环状RNA,并应用qRT-PCR方法在96例(复发和未复发各48例)验证出22个显著高表达的环状RNA。
该团队进一步结合列线图(Nomogram)数据挖掘方法,利用大样本的II/III期结肠癌患者队列(训练集,249例;内部验证集,122例;外部验证集,180例),最终构建了一组基于4个环状RNA(hsa_circ_0122319、hsa_circ_0008039、hsa_circ_0079480和hsa_circ_0087391)的分子指标模型(cirScore)。该分子指标模型预测II/III期结肠癌复发风险的准确性显著高于传统临床病理分期。首次揭示了一组由环状RNA组成的分子指标在中期结肠癌复发风险预测中的重要作用,并开创了基于机器学习的结肠癌分子标记物筛选新方法,为结肠癌的精准诊疗提供了新的思路和新的方法。
肝纤维化检测和治疗靶标
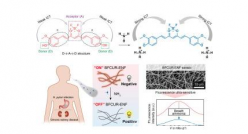
8月29日,南方医科大学丁彦青及周伟杰共研究将LECT2鉴定为孤儿受体Tie1的功能性配体,并为LECT2/Tie1信号在血管生成/血窦毛细血管化和肝纤维化中的潜在作用提供有价值的见解。临床相关性,血清LECT2水平可作为肝纤维化的潜在诊断标志物,并靶向LECT2/Tie1信号传导途径可以为治疗这种肝脏疾病提供新的途径。
具有免疫球蛋白样和表皮生长因子同源性(Tie)家族的受体酪氨酸激酶,包括Tie1和Tie2,在1992年首次报道。以往研究表明,Tie1和Tie2及其相互作用通过调节血管生成在人类疾病的发病机制中发挥重要作用。Tie1本身主要是血管生成的孤儿受体,但已被证明可以结合并调节Tie2的活性,因此在正常血管的发育和功能中发挥重要的作用。Tie1缺乏致由于严重的水肿、出血和微血管完整性丧失所致的脉管系统发育受损,进而出现了中晚期妊娠胚胎致死率。
白细胞衍生的趋化因子2(LECT2)是一种16kDa的分泌蛋白,最初被鉴定为中性粒细胞的趋化因子,可刺激软骨细胞和成骨细胞的生长。最近,越来越多证据表明LECT2参与许多病理状况,如败血症、糖尿病、系统性淀粉样变性,肝癌发生,非酒精性脂肪肝病(NAFLD)等。然而,LECT2在肝纤维化发展中的作用及其潜在机制仍然很不清楚。
研究表明,LECT2过表达抑制门静脉血管生成,促进血窦毛细血管化,并促进纤维化,而这些变化在Lect2敲出小鼠中被逆转。腺相关病毒载体血清型9(AAV9)-LECT2小发夹RNA(shRNA)处理显著减弱纤维化。LECT2的上调与晚期人肝纤维化分期相关。
该研究提出靶向LECT2/Tie1信号传导可能代表肝纤维化的潜在治疗靶标,并且血清LECT2水平可能是筛选和诊断肝纤维化的潜在生物标志物。
H3K4me3阅读器ZCWPW1在雌雄两性减数分裂进程中的作用
8月14日,香港大学深圳医院生殖医学研究中心刘奎教授研究团队与山东大学刘洪彬副研究员合作揭示了,蛋白H3K4me3修饰“阅读器”ZCWPW1在雌雄两性减数分裂中的不同作用。
研究发现Zcwpw1mRNA在小鼠中睾丸和胚胎卵巢广泛表达,减数分裂前期I就发生在这些器官中。在减数分裂前期I期间从细线期到圆形精子细胞阶段ZCWPW1蛋白表达升高(细线期和粗线期都是减数第一次分裂前期中不同时期),但在长形精子细胞中几乎检测不到。此外这些ZCWPW1蛋白只能在细胞核中检测到。免疫荧光实验进一步发现ZCWPW1蛋白从常染色体中消失,但仅出现在粗线期的精母细胞XY染色体中。雌形小鼠中发现从初级卵母细胞到粗线期阶段卵细胞的核区域也出现ZCWPW1蛋白。这些结果表明了ZCWPW1蛋白主要存在于减数分裂前期I的细胞核中发挥作用。
通过对联会复合体(SC)进行免疫染色观察减数分裂前期的染色体变化情况(联会复合体,synaptonemalcomplex)是减数分裂Ⅰ的偶线期中,配对的两条同源染色体之间形成的一种复合结构)。野生型小鼠在粗线期阶段精母细胞完全结合在常染色体上,约90.5%细胞的染色体配对结合成功;而在ZCWPW1敲除鼠中该阶段大多数的精母细胞并未结合在常染色体上,每个细胞上平均只有8个精母细胞配对成功。这就表明敲除ZCWPW1阻碍了精母细胞结合在常染色体。
本文发现ZCWPW1对雌雄两性减数分裂具有不同作用,Zcwpw1敲除雄鼠不育,精母细胞发育阻滞在减数第一次分裂偶线期,伴有DNA双链断裂修复异常,重组过程形成缺陷;而Zcwpw1敲除雌鼠早期可维持正常的生育力,只是呈现卵巢早衰(POI)的表型,重组过程出现延迟。本研究为阐释表观遗传调控在减数分裂中的作用及雌雄两性在减数分裂进程中的差异提供了证据。
细胞膜相关骨架结构调节细胞信号通路的机制
8月30日,庄小威教授实验室研究直接观察到了细胞膜受体与细胞膜下的蛋白骨架结构的相互作用,并验证这一相互作用对受体下游信号通路的调控机制。研究发现,在超分辨率显微镜下可以观察到多种细胞膜蛋白与MPS成分蛋白的共定位(Co-localization)。这些膜蛋白中包括G蛋白耦联受体CB1和细胞粘附分子NCAM1,而二者均已被证明可以间接激活络氨酸激酶受体(ReceptorTyrosineKinase,RTK)的功能。
进一步研究发现,在超分辨率显微镜下可观察到多种细胞膜蛋白与MPS成分蛋白的共定位(Co-localization)。这些膜蛋白中包括G蛋白耦联受体CB1和细胞粘附分子NCAM1,而二者均已被证明可间接激活络氨酸激酶受体(ReceptorTyrosineKinase,RTK)的功能。
晚期黏膜黑色素瘤一线治疗新方案
8月12日,北京大学肿瘤医院郭军教授团队发表一项免疫疗法联合抗血管生成靶向药物的晚期黏膜黑色素瘤一线治疗新方案。
北京大学肿瘤医院郭军教授团队围绕黏膜黑色素瘤基因组学、耐药机制和临床转化开展了一系列开创性研究工作,并于JClinOncol、NatCommun、ClinCancerRes等国际高水平期刊上发表了相应研究成果。同时,郭军教授还以黏膜黑色素瘤章节主编的身份,参与编写了国际权威教科书《皮肤黑色素瘤》(CutaneousMelanoma),彰显了我国学者在黏膜黑色素瘤领域的国际影响力。
科研人员对特瑞普利(重组人源化抗PD-1单克隆抗体注射液)联合阿昔替尼(VEGFR-TKI,抗血管生成的酪氨酸激酶抑制剂)在亚洲人群晚期黏膜黑色素瘤一线治疗中的安全性、耐受性、药代动力学等进行研究,证实特瑞普利联合阿昔替尼的客观缓解率可达60.6%,出现肿瘤退缩的患者达75.8%,而以往报道中黏膜黑色素瘤一线治疗的客观缓解率从未超过20%。
该研究提供了全球最前沿的晚期黏膜黑色素瘤中效率最高的一线治疗方案,有望成为国际黏膜黑色素瘤一线治疗的新标准。
分娩方式或在塑造儿童皮肤微生物组中起关键作用
近日,复旦大学生命科学学院的研究团队发现,儿童微生物组细菌菌属与其母亲的相比,与无关女性的细菌菌属更为相似。数据表明,分娩方式可能是塑造儿童微生物组的一个重要因素。
研究人员检查了158名1至10岁儿童皮肤微生物组的变化,分析其与微环境的关系,以及与其母亲微生物菌群组成之间的关系。其中50名儿童的母亲是随机挑选的,代表不同的儿童年龄组。使用16SrRNA基因扩增子测序比较了儿童与其母亲之间的微生物组结构。样本取自三个皮肤部位:脸颊中央、前臂四分之一处和小腿中部。根据年龄、性别和皮肤位置,将474个样本(每个儿童有3个皮肤位置)的数据汇集到36组中。
样本的部位与年龄是决定儿童皮肤细菌组成的主要因素,这三个部位之间存在显著的差异。然而,链球菌和颗粒细胞的丰度与年龄呈负相关。儿童中大多数细菌属的相对丰度与其母亲相比,与无关女性相比更为相似。10岁儿童的面部细菌成分与是否通过剖腹产或阴道分娩出生密切相关。
新型细胞器迁移体的产生机制及其生理功能研究取得新进展
为揭示迁移体的产生机制,俞立教授课题组与以色列特拉维夫大学课题组合作,发现Tspan4蛋白质及胆固醇在迁移体形成过程中发挥关键作用,提出了迁移体形成机制的模型,并进行实验验证,初步解释迁移体的形成机制:由于细胞迁移引发了Tspan4蛋白质及胆固醇在收缩丝上的局部高度富集,并因此增加富集区域膜的弯曲刚度,从而形成迁移体结构。
为阐明迁移体是否参与体内生物学过程,俞立教授课题组与孟安明院士课题组合作,发现斑马鱼早期胚胎发育过程中会产生大量的迁移体,并许多重要的信号因子包括趋化因子、形态素、生长因子等在迁移体里高度富集。他们鉴定出在斑马鱼早期胚胎中调控迁移体产生的重要基因tspan4a和tspan7,并构建了迁移体产生缺陷tspan4a和tspan7母源突变体。研究发现当迁移体产生被阻断后,斑马鱼会出现器官形态异常的表型,包括器官形态缺陷和左右不对称缺陷等,通过外源回补迁移体可以显著降低缺陷比例。进一步研究表明,迁移体会在胚盾空腔中聚集,通过释放内含趋化因子Cxcl12形成一个区域信号中心,保证背部先驱细胞紧密联系在一起,整体定向运动形成KV囊泡,从而调控各个器官原基在胚胎体内的正确空间定位及发育。
该研究一方面初步解释了迁移体的形成机制,另一方面发现了迁移体的生理功能,为理解斑马鱼胚胎发育提供了新的思路。相关成果近期在NatureCellBiology上同期发表。