前言
多形性胶质母细胞瘤(GBM)是成人最常见的原发性中枢神经系统(CNS)恶性肿瘤。目前所有的标准护理治疗对其均效果不佳,预后差,5年总生存率仅为6.8%。
GBM的治疗标准包括最大限度安全的肿瘤切除,然后是放疗(RT)和替莫唑胺(TMZ)联合化疗。与单纯放疗相比,联合治疗的中位总生存期(OS)分别为14.6个月和12.1个月。2015年,FDA批准了一种新的电物理治疗模式,即GBM患者的肿瘤治疗场(TTFields)。III期(NCT00916409)临床试验证明,TTFields治疗的中位无进展生存期(PFS)提高到6.7个月,而替莫唑胺组为4.0个月。中位OS也显著改善,分别为20.9个月和16.0个月(p<0.001)。
然而,几乎所有GBM都会复发。可用的治疗方案包括二线手术、放疗、烷化剂化疗和贝伐单抗治疗。不幸的是,从第一次进展或复发开始,中位OS的范围仅为6到9个月。因此,迫切需要新的治疗策略来治疗复发性GBM。
免疫疗法是一种利用患者自身免疫系统对抗肿瘤的新型疗法,它彻底改变了多种癌症的治疗方式,虽然到目前为止,免疫疗法在GBM的治疗还未取得突破,但值得注意的是,先前接受放疗和化疗治疗的复发性GBM通常具有更高的突变负荷,并且预期比未经治疗的GBM患者具有更高的免疫原性,这增强了人们对免疫治疗的信心和乐观态度。对其生物学、免疫微环境的进一步理解以及新的治疗组合方法的出现,可能会改变目前免疫疗法在GBM的困境。
中枢神经系统的免疫特权
长期以来,中枢神经系统一直被认为是一个免疫特权系统:由于血脑屏障(BBB)阻挡了病原体,CNS比任何其他器官接触病原体的机会要少得多。从在进化上,由于不需要经常发动免疫攻击,而且对脑细胞自动免疫的后果,抑制中枢神经系统的免疫可能是有利的。
直到2015年,人们普遍认为中枢神经系统缺乏功能性淋巴管。由于这些是免疫反应的重要组成部分,因此很难理解抗原呈递是如何发生的。另外,BBB本身也被认为是有效免疫反应的限制因素,因为它的紧密连接在物理上阻止了免疫参与者(如淋巴细胞或抗体)的进入。
中枢神经系统和其他器官之间的一个关键区别在于大脑中几乎没有用于抗原呈递的树突状细胞。在中枢神经系统中,小胶质细胞被认为是主要的抗原呈递群体,它主要为抗炎表型,使T细胞倾向于免疫抑制Th2表型。
然而,现在已经有许多确切的证据表明,主动免疫监测确实发生在中枢神经系统中,并且针对感染产生有效的免疫反应。此外,多发性硬化症等自身免疫性疾病也表明,免疫原性抗原可以在中枢神经系统中被处理并触发强大的免疫反应。2015年,沿硬脑膜静脉窦通向颈深淋巴结的淋巴通路的发现极大地改变了我们对大脑免疫环境的概念。今天,虽然中枢神经系统被认为是一个免疫学上与众不同的部分,但人们相信它的免疫微环境为针对脑肿瘤的免疫治疗提供了合适的条件。

GBM的免疫逃避机制
GBM是最致命的脑癌,生长迅速,复发频繁,这一事实可归因于多个因素,包括高增殖率、高组织侵袭能力、抗治疗的癌症干细胞以及药物难以进入中枢神经系统。除此之外,免疫逃避在GBM预后不良中也起着关键作用。
许多免疫逃避机制参与其中,包括通过完整的血脑屏障阻止免疫细胞进入,肿瘤微环境的免疫抑制,或通过劫持关键免疫途径和参与者,如免疫检查点受体表达、调节性T细胞、肿瘤相关巨噬细胞的调节。
GBM具有对免疫攻击很高的内在抗性机制以及出色的适应能力,一项关于GBM中PD-1阻断的研究显示,只有少数患者出现初始反应,并且所有患者都复发。复发肿瘤活检的病理学表现为免疫抑制分子的新表达和新抗原表达的丢失。
首先,GBM从其在中枢神经系统中的位置获得免疫抑制特性。其次,GBM受益于肿瘤组织的复杂异质性。此外,GBM还受益于有利的微环境,甚至进一步使其具有免疫抑制作用。一项研究表明,针对中枢神经系统抗原的CD8+T细胞在进入中枢神经系统后被迅速清除,证明了中枢神经系统微环境的耐受作用。在炎症环境中,干扰素诱导的趋化因子激活内皮细胞并允许外周免疫细胞穿过BBB。GBM则通过上调基质中的化学吸引蛋白并从外周招募MDSC和TAM等抑制性单核细胞来逃避免疫作用。
最后,GBM免疫治疗的一个障碍是医源性免疫抑制。在GBM中,放射治疗与替莫唑胺联合化疗是标准治疗方法。一项研究表明,这种治疗导致3/4的患者的CD4+T细胞计数下降到300细胞/mm3以下。此外,替莫唑胺在PD-1阻断的临床前试验中阻止了记忆T细胞的诱导产生。
肿瘤疫苗治疗
与用于预防传染病的预防性疫苗一样,抗癌疫苗由添加了佐剂的肿瘤抗原组成,以期触发和增强免疫反应。在GBM中考虑了三种主要方法:(1)肽/DNA疫苗;(2)DC疫苗;(3)mRNA疫苗。
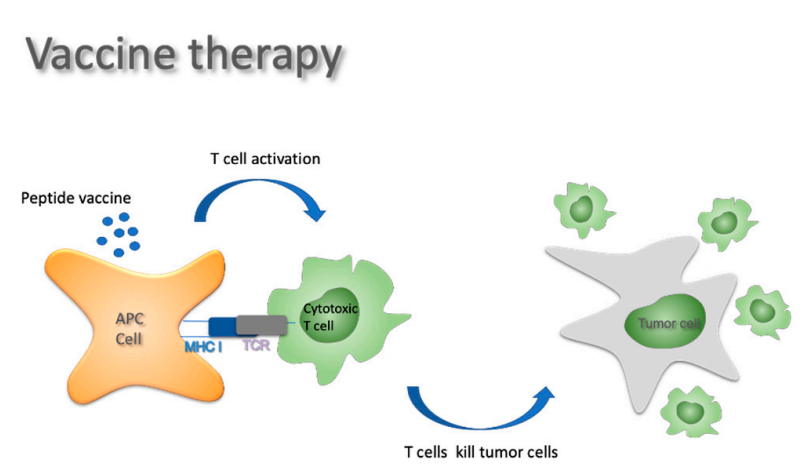
最早也是评估最多的疫苗方法之一涉及EGFR的选择性剪接变体III(vIII),它是由外显子2到7的选择性剪接产生的肿瘤特异性抗原。EGFRvIII在25–30%的GBM肿瘤中表达。Rindopepimut(CDX-110)是研究最广泛的EGFRvIII肽疫苗。它使用免疫调节蛋白KLH作为佐剂,其在2015年2月被FDA认定为GBM的“突破性疗法”,II期数据显示,与对照相比,PFS和OS有均所改善。
为了提高对GBM产生有效免疫反应的几率,人们将多种肿瘤特异性抗原结合到一种疫苗中。IMA950是一种肽疫苗,它结合了11种GBM衍生抗原,该疫苗已被证明能诱导T细胞对单个和多个抗原的反应。然而,目前还没有进行随机临床试验,因此这种免疫反应是否确实导致临床结果的改善还有待证明。
树突状细胞是一种强大的抗原呈递细胞,能够诱导抗原特异性T细胞应答。迄今为止,已有两项随机试验评估了DC疫苗的疗效。ICT-107是一种针对肿瘤和癌症干细胞六种抗原的自体DC免疫疗法,包含MAGE-1、AIM-2、HER2/neu、TRP-2、gp-100和ILRa2。在一项涉及124名患者的双盲、安慰剂对照试验中,75名患者在RT和伴随TMZ后接受ICT-107治疗。结果显示,治疗组的PFS中位数略高于对照组(11.2个月vs 9个月;HR:57,p=0.011),但OS无差异(17.0个月vs 15个月;HR:0.87,p=0.580)。有趣的是,与无应答者相比,具有免疫应答的患者显示出改善的PFS和OS。另一个DC疫苗DCVax-L进行的大规模、随机和对照III期试验(NCT00045968)的结果显示,与历史对照数据相比,中位OS达到23.1个月。
此外,还有许多候选疫苗仍在开发中:NCT02287428临床试验正在测试包含多达20个长肽的个性化的新抗原肽疫苗。NCT03422094试验正在研究NeoVax与ipilimumab或nivolumab的联合应用。GAPVAC-101基于30种GBM过度表达抗原的个性化疫苗正在1期临床中(NCT02149225)。
溶瘤病毒
在GBM中已研究了几种OV的疗法,包括腺病毒、麻疹病毒、脊髓灰质炎病毒、HSV、细小病毒和逆转录病毒载体,并证明了该方法的可行性和安全性。最近,在GBM的1/2期临床试验中显示了新型OVs显著的疗效,患者亚群的生存期超过3年。这些包括腺病毒DNX-2401(Ad5-delta24-RGD)、麻疹病毒MV-CEA、细小病毒H-1(ParvOryx)、脊髓灰质炎鼻病毒嵌合体(PVSRIPO)和逆转录病毒载体Toca 511(vocimagene Amirepreprevec和Toca FC)。

Toca 511是一种基于小鼠白血病病毒的逆转录病毒载体,编码转化5-氟胞嘧啶(5-FC)的酵母胞嘧啶脱氨酶。在一项I期试验中(NCT01470794)测试了Toca 511在56例复发的胶质母细胞瘤患者中的疗效,中位OS为14.4个月,1年和2年的OS率分别为65.2%和34.8%。5名患者表现出完全缓解。Toca5试验是另一项多中心、随机、开放标签的II/III期与标准治疗比较的临床试验,但该试验于2020年因缺乏疗效而终止(NCT02414165)。
DNX-2401(Ad5-Delta-24-RGD;tasadenoturev)是一种肿瘤选择性溶瘤腺病毒载体。肿瘤细胞靶向是通过删除E1A蛋白中的24个碱基对并在病毒衣壳蛋白中插入Arg–Gly–Asp(RGD)基序来实现的,从而增加对αV整合素的亲和力。在1期共37例复发性恶性胶质瘤患者的1期剂量递增试验中,20%的患者在治疗后存活超过3年,其中3名患者的PFS超过3年。治疗后活检显示DNX-2401可在肿瘤内复制,并诱导有效的肿瘤内CD8+和T-bet+T细胞浸润,另一项II期联合试验正在进行中,该试验旨在研究48例复发性GBM患者肿瘤内注射DNX-2401和全身给药pembrolizumab的疗效(CAPTIVE/KEYNOTE-192,NCT02798406)。中期结果显示中位OS为12个月,6个月OS率为91%, 47%的患者显示有临床益处(病情稳定或消退)。四名患者有PR,其中三名患者存活时间>20个月。
其他腺病毒载体也正在研究中。一期临床试验(NCT02026271和NCT03330197)正在测试肿瘤内注射Ad-RTS-hIL-12,这是一种在激活性配体veledimex存在下表达人IL-12的可诱导腺病毒载体。NCT02026271试验是一项剂量递增试验,在38例复发或进展性胶质瘤的成年患者中进行,显示出良好的安全性和生存率(中位OS为12.7个月)。NCT03330197试验是其尚未完成的儿科试验,该试验仍在招募中。
麻疹病毒Edmonston疫苗株是一种安全、特异的溶瘤病毒,经基因改造后可表达人类癌胚抗原(CEA)作为报告基因,用于监测体内病毒复制。MV-CEA OV已在23名GBM患者的一期临床试验(NCT00390299)中进行测试,分别在手术前和手术后给予,两者的中位OS分别为11.4和11.8个月,6个月的中位PFS率为22–23%。
ParvOryx是一种改良的大鼠细小病毒,在一项I/IIa期剂量递增试验(NCT01301430)中,在18例复发性GBM患者中进行了测试。ParvOryx治疗后中位OS为15.5个月,8名患者存活>12个月,3名患者存活>24个月,对肿瘤活检的分析显示,6名患者出现了强烈的CD8+和CD4+T淋巴细胞浸润。
PVSRIPO 是一种工程化的萨宾1型脊髓灰质炎减毒病毒,2016年5月,其获得了FDA的突破性疗法认定。在对61例复发性IV级恶性胶质瘤患者进行的I期剂量递增试验(NCT01491893)中,所有61名患者的中位OS为12.5个月,但安全性存在争议,因为19%的患者有3级或更高级别的不良事件。此外,大约20%的患者在PVSRIPO给药后能存活57-70个月。目前正在进行一项关于PVSRIPO单独或联合lomustine治疗复发性IV级恶性胶质瘤患者的随机II期试验(NCT02986178)。
其他几项针对复发性胶质母细胞瘤/胶质瘤成年患者的临床试验正在进行中,例如基于痘苗的OV TG6002联合5-FC(ONCOVIRAC,NCT03294486)的I/II期试验;表达免疫刺激OX40配体(OX40-L)的腺病毒OVDNX-2440的I期试验(NCT03714334);一项名为M032(NCT02062827)的表达IL-12的基因工程化单纯疱疹病毒(HSV-1)的I期试验;基因工程化HSV-1rQNestin34.5v.2与环磷酰胺联合的I期试验(NCT03152318)。
总的来说,这些早期临床试验表明OVs可以提高部分亚群患者的生存率。
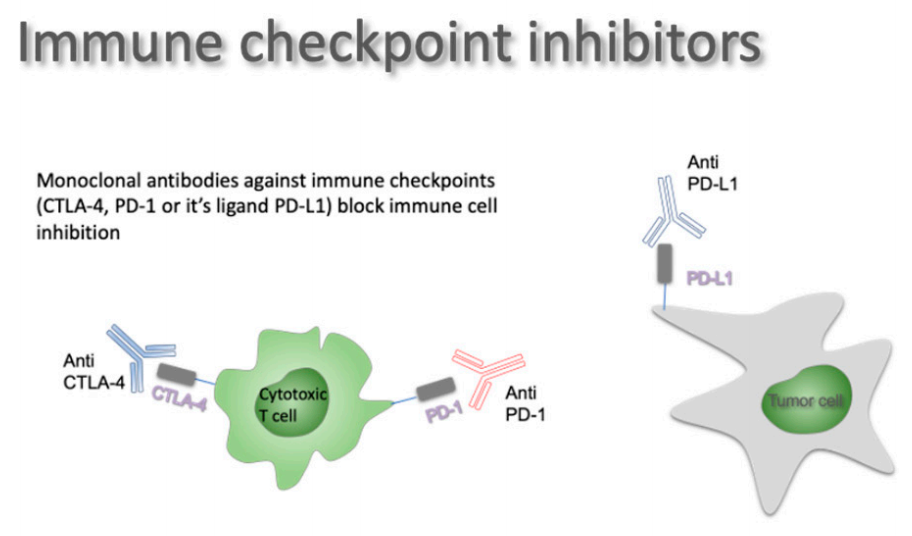
免疫检查点抑制剂
88%的新诊断胶质母细胞瘤和72%的复发胶质母细胞瘤显示PD-L1过度表达,尽管总体水平较低。因此,复发性GBM中的抗PD-1 ICI是许多I期临床试验的主题(NCT02017717、NCT02336165、NCT02337491、NCT02054806),总体显示抗PD-1或抗PD-L1单一疗法的应答率在2.5%到13.3%之间。6个月的PFS率在16%到44%之间,OS率在7到14个月之间。
CheckMate-143(NCT02017717)试验研究了nivolumab单药和ipilimumab联合应用对首次GBM复发患者的疗效。结果显示,单独使用nivolumab比组合方案显示出更高的中位OS(10.4个月vs 9.2个月),毒性更低。双检查点抑制在超过50%的患者中引发严重不良事件,因此这种方法不再被采用。
CheckMate-143试验的第三阶段比较了nivolumab 3和bevacizumab,然而由于缺乏疗效而提前终止,两组在中位OS和毒性方面均无统计学差异。目前,两项正在进行的III期试验正在研究nivolumab治疗新诊断的GBM:CheckMate-548试验(NCT02667587)正在测试替莫唑胺加放疗联合nivolumab治疗新诊断的MGMT甲基化GBM患者,(NCT02617589)正在研究联合放疗后nivolumab与替莫唑胺的对比。然而到目前为止获得的信息表明,这两项试验可能都不会达到其主要终点。
Keynote-028试验(NCT02054806)研究了另一种抗PD1抗体pembrolizumab对几种晚期实体瘤的疗效,包括26例胶质母细胞瘤患者。其中,一例PR(4%),12例(48%)SD,中位PFS为2.8个月,中位OS为14.4个月。
另一项II期试验研究了durvalumab作为单一疗法或与bevacizumab或放疗联合治疗30例复发性胶质母细胞瘤患者的疗效。4例PR(13.3%),14例SD(46.7%),6个月时PFS率为20%。
过继性细胞疗法
在GBM中,一项先导性试验研究了六名胶质瘤患者的自体TIL输注。3例为间变性星形细胞瘤,3例为GBM。在3名GBM患者中,2名患者表现出PR。在另一项临床试验(NCT00331526)中,使用淋巴因子激活杀伤(LAK)细胞治疗GBM,LAK细胞是一种异质性细胞群,主要由自然杀伤细胞(NK)和自然杀伤T细胞(NKT)组成,显示出不受限制的MHC抗肿瘤活性。共有33名患者在肿瘤切除腔内接受辅助性LAK细胞输注,平均OS为20.5个月。

CAR-T是目前肿瘤免疫治疗火热的领域,一些针对胶质母细胞瘤的CAR-T疗法正在开发中。常见的靶点包括新抗原IL-13R-α2、EGFRvIII、巨细胞病毒(CMV)双特异性受体和HER2。
在一项试点试验(NCT02209376),用单剂量的EGFRvIII特异性CAR-T细胞治疗了10例复发性EGFRvIII阳性GBM患者。然而这项试验没有显示任何临床益处,但有趣的是,治疗后的活检显示胶质母细胞瘤病变被CAR-T细胞浸润,证明它们能够穿过BBB。
GBM的CAR-T细胞研究非常火热:正在进行的GBM CAR-T细胞临床试验包括EGFRvIII(NCT01454596、NCT02209376、NCT02844062和NCT03283631)、EphA2(NCT02575261)、HER2(NCT02442297、NCT01109095和NCT03389230)、IL-13Rα2(NCT02208362)和PD-L1(NCT02937844)。此外,新的潜在靶点正在临床前模型中出现,如CD70、IL-7受体和PDPN。
迄今为止发表的临床试验表明,CAR-T细胞确实可以浸润GBM肿瘤,并可以消除显著的肿瘤体积,但它们也证明了GBM的强大适应性,使其能够逃避免疫攻击。异质性抗原表达、免疫抑制肿瘤微环境和免疫编辑是CAR-T细胞有效性需要克服的主要障碍。这些障碍并不局限于GBM,实际上,CAR-T细胞在实体瘤中的疗效尚未得到证明。通过强化CAR-T细胞的设计可能克服这些挑战,最近,设计了一种靶向三种胶质瘤抗原(IL13Rα2、HER2和EphA2)的三价CAR-T细胞,几乎可以识别100%的GBM。CAR-T细胞设计的这些进展与检查点抑制剂或溶瘤病毒等免疫治疗策略相结合,可能是GBM免疫治疗成功的关键。
挑战与展望
迄今为止,还没有任何一种免疫治疗方法能够在随机III期试验中令人信服地显示出显著的临床益处。这可能与许多因素有关,包括肿瘤限制因素:如GBMs的突变负荷较低,为免疫系统提供的治疗靶点较少;抗原靶点在癌细胞中选择性下调;此外,GBM可能在其发育过程中受到显著的免疫编辑,导致高度免疫回避和抑制性的肿瘤。GBM的肿瘤微环境特别具有免疫抑制作用,人们对CSF-1(NCT02526017)、TGF-β(NCT02423343)和IDO(NCT02052648)的抑制和重新编程进行了研究,但迄今为止没有临床益处。
此外,GBM患者免疫系统的正常功能可能会受到所需支持治疗(如类固醇)或化疗的毒性作用阻碍。临床研究选择不需要类固醇的患者,至少在治疗的第一阶段,可能是至关重要的。在新诊断的GBM患者中,在放疗和替莫唑胺治疗之前,甚至在神经外科切除病灶之前考虑新辅助免疫治疗可能也很关键。II期随机试验中观察到,与仅在辅助治疗环境下治疗的患者相比,切除前服用pembrolizumab可显著改善OS。
考虑到后续的免疫治疗,局部治疗策略的选择可能也很重要:临床前数据表明,局部治疗方式,特别是立体定向放射治疗,确实通过释放肿瘤抗原与免疫治疗发生协同作用。这一理论基础是两项正在进行的临床试验(NCT02648633和NCT02866747),将立体定向放射治疗与GBM PD-1抑制相结合,以及一系列结合不同抗原释放的局部治疗(NCT02311582、NCT01811992、NCT02197169、NCT02798406和NCT02576665)。
最后,单一的免疫治疗方法很可能不足以引起足够强烈的反应。因此,正在积极研究联合疗法,希望克服GBM中的免疫抑制环境和肿瘤逃逸机制。
小结
免疫疗法彻底改变了癌症治疗的模式,然而,GBM已经证明对肿瘤免疫攻击的所有阶段具有强大的抵抗机制。许多因素可以解释迄今为止获得的阴性结果,在肿瘤发展过程中,GBM可能受到显著的免疫编辑,导致高度免疫抑制和逃避表型。
到目前为止,对于GBM产生免疫治疗抵抗或肿瘤固有特性的了解还很少。进一步研究GBM肿瘤及其微环境中决定免疫治疗反应的分子因素至关重要,并且有必要重新考虑评估免疫治疗方法的临床试验设计,以快速获得有关这些方法潜在临床影响的信息。目前,从最新的数据来看,免疫治疗方法的联合应用可能是最终在GBM免疫治疗获得突破的出口。
参考文献:
1. Immunotherapy in Glioblastoma:A Clinical Perspective. Cancers (Basel). 2021 Aug; 13(15): 3721.
原文标题 : 胶质母细胞瘤的免疫治疗前景