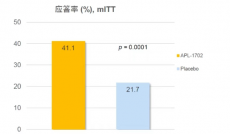
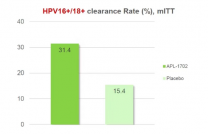
随着更多省市组织开展HPV接种优惠政策,“馨可宁”作为目前的国产“独苗”,将率先受益于HPV接种宣传以及市场渗透,同时也为未来其他产品的上市做了品牌铺垫。但群雄环伺,疫苗的竞争远没有结束。


“馨可宁”帮助钟睒睒在疫苗赛道撕开了一个不小的口子。
因为二价HPV(宫颈癌)疫苗(即“馨可宁”)供不应求,钟睒睒旗下的万泰生物2021年业绩爆表。全年营收同比增长144.25%,归属上市公司股东净利润更是同比大增197.83%。
这还没完。
2022开年不久,随着河南郑州、河北石家庄、海南、重庆、福建等地陆续加入HPV疫苗(主要是国产疫苗)免费接种的行列,作为国产“独苗”的“馨可宁”竞争力更加凸显。
不过,沃森生物们的进度在时刻提醒钟睒睒,竞争远未结束。
01
戊肝疫苗受挫,二价HPV疫苗突围
实际上,钟睒睒的疫苗之路走得并不平坦。
在二价HPV疫苗上市之前,万泰生物的戊肝疫苗先于2012年面世,即“益可宁”。“益可宁”从研发到上市,用了14年。而且是全球独家产品,被两院院士评为2012年度“中国十大科技进展”。
但是很多人听过甲肝、乙肝甚至丙肝,对戊肝却还不熟悉。由于人们对戊肝疫苗的认知程度低,益可宁上市后销售不及预期,2019年销售收入仅有1496.64万元,占当年营收的1.26%。
与戊肝不同,宫颈癌疫苗是全球唯一预防癌症疫苗品种,宫颈癌也是女性主要的健康隐患之一。戊肝疫苗受众小、认知程度低的问题,在HPV疫苗上消失不见。
世界卫生组织发布的《加速消除宫颈癌全球战略》提出,到2030年要实现全球 90% 的女孩在15岁之前完成 HPV疫苗接种,通过疫苗接种、筛查和治疗等三级防治路径,推动全球实现消除宫颈癌的目标。目前已经有包括中国在内约200个国家响应。
在“馨可宁”上市之前,默沙东的四价和九价HPV疫苗、GSK的二价HPV疫苗均已进入中国市场。得益于很多媒体、自媒体的科普,不少人或多或少都了解一些HPV疫苗相关知识。不过进口疫苗“一针难求”,加价购买、排队预约成为常态。
在此背景下,后来者“馨可宁”不需要市场培育,可直接依靠低价“攻城略地”。在9-14岁人群中,“馨可宁”的“两针法”优于竞争对手的“三针法”,在价格上仅相当于GSK二价产品的38%。
“馨可宁”在2019年末获批上市后,万泰生物2020年归母净利润同比大增224.13%,2021年则延续了势头。帮助万泰生物摆脱了其他疫苗和试剂企业面临的“疫情后遗症”,市值维持在1500亿元。
业务结构也得以扭转,万泰生物疫苗收入占比在2020年达到37.04%,2021H1进一步提升至41.78%。
未来随着更多省市组织开展HPV接种优惠政策,“馨可宁”作为目前的国产“独苗”,将率先受益于HPV接种宣传以及市场渗透。同时也为未来其他产品的上市做了品牌铺垫。
02
群雄环伺,地位不稳
2月11日,万泰生物盘中跌停。
原因是,前一日沃森生物子公司申报的二价HPV疫苗的上市申请审评审批状态已更新为“在审批”。这意味着该疫苗有望不久后正式获批,成为第二款获批上市的国产二价HPV疫苗。
沃森生物曾表示,其二价HPV疫苗生产线的设计年产能为1500万剂左右。若审批顺利,或将从各地免费接种中“分一杯羹”。
这只是疫苗行业竞争的一个侧面。面对消灭宫颈癌的目标,关于国产HPV疫苗的角力,才真正开始。
据“药智网”文章,我国4价HPV疫苗领域,开展临床的产品有3家。目前进展最快的是北京、成都生物制品研究所产品,已经进入三期阶段。9价HPV疫苗领域,博唯生物、康乐卫士、瑞科生物及万泰生物这四家企业已经进入三期临床阶段。
在更高价产品上,中国生物所在研的 11 价 HPV 疫苗已经进入临床二期阶段,浙江普康在研的 16 价 HPV 疫苗也已经处于临床一期阶段。
当然,万泰生物的九价HPV疫苗在国内走在前列,是国内首个申报临床的国产九价HPV疫苗。华西证券预计,如果进展顺利,该疫苗有望于2024年底或2025年初获批上市。
万泰生物也为九价HPV疫苗上市做足准备。
在最近的定增方案中,万泰生物拟募资不超过35亿元,计划将其中11亿元用于九价宫颈癌疫苗二期扩产建设项目。项目完成后,万泰生物将拥有6条基于大肠杆菌技术平台的HPV 9价类病毒颗粒(VLP)疫苗原液生产线,设计产能可增加至6000万支/年。
不过,当前该定增尚未通过,而且受到部分投资者和媒体质疑。三期临床能否成功也是未知。在产品获批上市之前,万泰生物能否抢占先机仍无定数。
已上市的默沙东九价HPV疫苗的威胁也还在。
在去年11月的调研中,有机构就“默沙东九价HPV疫苗三期临床研究注册检查顺利完成,年龄要扩容到9-45岁”提问,万泰生物对此依然乐观,理由是HPV疫苗目前仍然供不应求。
除此之外,当时市场也有担心HPV疫苗从“二类苗”转为“一类苗”,也就是从公民自费自愿接种,到政府免费提供。届时可能会带来类似药品集采的影响,疫苗价格下降。
除了HPV疫苗,万泰生物布局的产品还有两款水痘疫苗和一款鼻喷新冠疫苗。
其中,水痘疫苗是预防水痘的唯一手段,但我国西部接种率仅有41%。而且我国多地已经逐步改变过去的“一针法”,推进“两针法”。根据万泰生物公告,目前冻干水痘减毒活疫苗(V-Oka株)已完成临床三期试验,预计2022-2023年获批上市。原创的新型水痘疫苗(VZV-7D)已进入二期临床试验,预计2025年获批上市。鼻喷新冠疫苗则处于三期临床试验中。
03
研发平台构筑实力,会计变更需警惕
万泰生物疫苗研发的核心竞争力,是其所创建的、全球独有的大肠杆菌原核表达类病毒颗粒疫苗技术体系。
招股书介绍,不同于酵母、昆虫细胞杆状病毒真核表达系统,该技术体系生产成本低、效率高、规模易于放大、安全性高,同时又结合了病毒样颗粒疫苗免疫原性好,安全性高的特点,达到生产效率与免疫效果的完美结合。
良好的通用性,又使得该体系能够适用于多种不同病原体疫苗的开发。万泰生物已上市的戊肝疫苗、二价HPV疫苗,以及在研的九价HPV疫苗,均基于该技术体系。
2019年9月,万泰生物子公司万泰沧海,与国际顶尖疫苗企业GSK签署合作开发协议。
根据该协议,GSK将支付共计 1.34 亿欧元里程碑款(约合 10 亿元人民币),用其宫颈癌疫苗抗原技术开发新型宫颈癌疫苗,并同万泰生物分享国际市场销售收入。里程碑付款共分八次,目前万泰沧海已经收到GSK两笔里程碑付款。这说明万泰沧海的技术被GSK所认可。
但是在技术之外,需要注意万泰生物在会计处理方面的改变。
去年12月24日,万泰生物发布《关于会计估计变更的公告》:本次会计估计变更前,公司基于谨慎性原则将内部药品研发项目的所有支出于发生时计入当期损益。
变更后,药品研发进入三期临床试验阶段前的所有研发支出划为研究阶段支出,药品研发进入三期临床试验阶段后的所有可直接归集研发支出归为开发阶段支出。
根据会计政策,研究支出阶段发生的费用全部计入损益;开发阶段的支出在满足特定条件时,可以进行资本化处理,不符合条件的支出才计入损益。
由于三期临床试验耗费不低,如此会计估计变更,企业可以通过研发资本化来“减少”费用,“提升”业绩。
而这对于有多款疫苗进入临床三期或之后的万泰生物来说,有些敏感。
本文作者 | 张贺
来源 | 英才杂志
end
原文标题 : 首富钟睒睒的疫苗“战事”