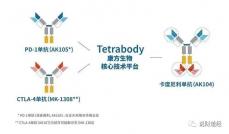
如果说双抗药物是单抗药物升级后的下一代,那么PEG双链接子技术就是传统PEG单链子技术的新一代升级。
PEG双链接子技术的出现,不仅让难以突破的双抗ADC变成现实,还让“三抗”(三重免疫作用)药物成为了可能。
什么是PEG?PEG技术在药物开发过程中扮演着怎样的角色?为什么抗体药市场迟迟没有出现双抗ADC和“三抗”药物?PEG双链接子技术为何能够改变这一局面?带着这一系列的问题,动脉网(微信号:vcbeat)专访了深圳康源久远生物技术有限公司(简称:康源久远)创始人刘树民博士,该公司也是目前世界上唯一一家拥有PEG末端双特异性链接子专利的公司。

康源久远创始人 刘树民博士
1历史:PEG耦合蛋白质,长效药登上时代舞台
PEG即聚乙二醇,是新药开发中广泛使用的一种成分。
上世纪60年代末,由于市面上还未出现DNA重组技术,科研人员在制备药物时常使用动物来源的蛋白质,这导致出现了严重的免疫原性问题。美国新泽西罗格斯大学的Davis教授在新药研发时,将临床上作为辅料广泛使用的PEG耦合到蛋白质上,从而降低了免疫源性,延长了半衰期。这就是长效药的雏形。
这种将PEG耦合到蛋白质的行为又称之为蛋白质的聚乙醇化,其本质是一种药物输送技术。
将活化的PEG与蛋白质分子偶联,可以改善蛋白质的三维空间状态,致使蛋白质的各种生物化学性质发生改变,包括能够让蛋白质的溶解度及化学稳定性增加、抵抗蛋白酶水解的能力提高、免疫原性和毒性降低或消失、体内半衰期延长、血浆清除率降低等。
1981年,Davis教授和他研究生Abuchowski一起成立了基于蛋白质聚乙醇化的生物医药公司Enzon(安龙);1990年,Enzon开发的全球首个蛋白质聚乙醇化药物ADAGEN获得FDA批准上市;紧接着,1994年Enzon开发的第二个聚乙醇化药ONCASPAR又获批上市。
2000年Schering-Plough(先灵葆雅)的新药PEGINTRON、2002年Roche(罗氏)的新药PEGASYS等都是采用Enzon的聚乙醇化技术开发的药物。截止目前,FDA批准的聚乙醇化药物有20个。聚乙醇化药物成为除了单克隆抗体以外成药性最高的一个药物开发技术。
值得一提的是,康源久远的创始人刘树民博士正是来自于Enzon公司,并在该公司工作了13年,曾带领团队完成了包括第二代ONCASPAR(ASPARLAS)和ADAGEN (REVCOVI)在内的多个聚乙醇化药物的研发、生产、技术转移和FDA报批。
康源久远另一位联合创始人乌德春是刘树民博士在Enzon公司的同事,有机合成专家。乌德春在Enzon工作近20年,主要负责聚乙醇化的链接子设计开发,参与过多代链接子技术的升级,同时是多个专利的发明人。
刘树民博士介绍道,在Enzon工作期间,他和乌德春一起合作多个蛋白质聚乙醇化化项目,乌德春负责PEG链接子,刘树民博士负责蛋白质聚乙醇化,二人工作上相辅相成,协作共进。这也为未来二人齐心协力创建康源久远打下了良好的基础。
2创新:攻克双抗药物轻重链错配难点,PEG单链接升级双链接子
在过去30年里,聚乙醇化技术的进步主要表现链接子技术的进步上,从最早期的非特异性链接,到定点特异性链接,再到可以降解、缓释的连接子技术,这些都是PEG通过一个化学链接子与一个药物靶点结合的形式。

PEG技术的发展
2013年,关于双特异抗体(双抗)的临床试验数据逐步被报道,双抗药物的开发变得火热了起来。刘树民博士和乌德春一直关注着肿瘤抗体药领域的发展,自然注意到了双抗药物开发的技术难点——在双抗药物制备过程中,由于两个原始抗体的重链、轻链之间的错配,会产生难以分离的杂质,从而到导致药物开发及纯化变得异常困难。
“当时我们就想,如果能够开发出两个链接子,分别一对一特异性连接到两个抗体片段上,就有机会避免杂质的产生,攻克这个技术难点。”刘树民博士告诉动脉网。
带着这个idea,刘树民博士和乌德春在2015年底美国新泽西州建立了实验室“普林斯顿久远(PEB)”,专门开发这种双抗技术;2017年,二人基于擅长的PEG技术完成了双链接子的开发,并申请了PEG末端双特异性链接子专利,成为目前世界上唯一拥有该专利的共同发明人。
这种PEG双链接子技术能够通过链接子的特异性在体外按照顺序链接结合到不同靶点的抗体片段,巧妙地避开了因错配导致的杂质,提高药物开发的成功率。
2018年7月,刘树民博士和乌德春的研发成果受到了分享资本的关注,遂引荐二人来到深圳成立了康源久远。同时,康源久远完成了对美国PEB的收购,PEB成为康源久远的全资子公司。

康源久远的发展历程
3应用:PEG双链接子技术蓝图,助力实现双抗ADC、三重免疫等
如果说康源久远的初心是解决双抗药物的轻重链错配问题,那么在后续关于PEG双链接子技术的研究,让团队找到了该技术更广阔的应用前景。
运用两个特异性不同的链接子对现有药物靶点进行组合,拓展了现有药物靶点的应用,并能够成功克服原有药物研发领域的一些技术壁垒,例如双抗ADC、三重免疫等。康源久远基于该技术依照分子的组合,布局了三大专利领域。

PEG双链接子技术的三大应用
如果是连接两个抗体片段scFv就形成了利用PEG代替Fc的双抗技术平台;如果连接抗体、细胞因子组成的重组蛋白,就形成了多重免疫药物的开发技术;如果用一个链接子连接小分子药物,另一个链接子连接一个scFv的双抗,就形成了双抗ADC药物。
这是康源久远基于PEG双链接子技术开发的三个主要应用场景。未来,公司将会利用该技术对现有的靶点做出更多的组合,开发出更多的药物。
>>>>
双抗ADC
ADC即抗体偶联药物。到目前为止,市面上仅有8款单抗ADC药物落地,双抗ADC还没有获批上市的药物。而在临床研究上,只有不到5款的双抗ADC正在进行不同阶段的前期临床试验。
极少的双抗ADC进入临床,其大部分原因在于ADC制备过程中,追求高药物/抗体比(DAR)会导致药物在体内的不稳定,从而造成毒性增强;其次疏水性小分子细胞毒化合物也会直接影响ADC的其它各类重要属性,而用现有的偶联技术得到的双抗ADC对药物的成药性,体内的稳定性、毒性、内吞等都有不同程度的负面影响。
不过康源久远的PEG双链接子技术刚好可以解决这些技术难题:应用双抗ADC技术把药物连接在PEG上,将形成的聚乙醇偶联药物再与双抗连接,这样就可以克服传统制备及应用ADC的不足。
刘树民博士表示,目前康源久远的该项技术正处于开发阶段,初始的数据已经表明研究方向和路线的正确性。
>>>>
三重免疫
单抗药物治疗实体瘤的临床响应率低一直是医疗界的一大痛点,以乳腺癌为例,单药赫赛汀的临床响应率约18%,剩余近80%的患者无法受益于该种抗体药治疗,让更多的患者受益于抗体疗法的治疗成为临床上亟待解决的一个技术难题。
事实上采用抗CD3/抗PDL1的双特异性抗体可以增强免疫杀伤作用,提高患者的临床响应率。然而由于抗CD3/抗PDL1双特异性抗体同时采用了高效杀灭癌细胞的重导T细胞效应和免疫检查点阻断效应(PD1/PDL1),一些表达PD-L1的正常组织细胞细胞,如内皮细胞、巨噬细胞、NK细胞等也可能会被杀灭,从而导致毒副作用的产生,以及降低抗肿瘤效应。
为了解决抗CD3/抗PDL1可能产生的毒副作用,康源久远引入了两个细胞因子“帽子”,通过屏蔽抗体的活性结合部位,使药物不能对正常组织中表达PD-L1的细胞产生杀灭作用,从而达到避免毒副作用的效果。
康源久远设计的三重免疫治疗药物的结构,包括了高效免疫杀伤作用的T细胞重导效应、免疫检查点阻断治疗效应、细胞因子免疫治疗效应。三重免疫作用具有协同作用,最终达到“1+1+1>3”的效果。
据悉,康源久远已启动了A轮融资,计划募集资金6000万人民币,主要用于核心管线的中美双报、后续产品的研发,以及推进临床一期试验。
作者:王婵