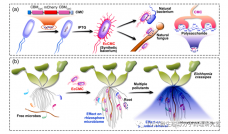
其中,设计是指根据目标产物设计合理的基因通路,利用细胞内部天然既有或外源补充的物质合成目标化合物,即原料在多种酶的作用下转化为目标产物的过程。构建是指根据设计的基因序列制造出相应的DNA片段并确保基因通路在活细胞中如预期地工作。测试是指搭建完成细胞工厂后,对细胞状态、中间产物浓度和终产物浓度等多项指标进?评估。随后,根据测试结果的反馈对设计进行优化迭代,最终获得目标产物的细胞工厂。
从实验室到工厂,合成微生物解决的不只是化合物合成成本的问题,而且超越传统化学工艺,正在创造全新的分子和材料。李腾博士指出,“就像集成电路转变了信息处理的方式一样,合成微生物也将改变人们在未来如何获取新分子和新材料”。
合成生物技术产业化进程加快
合成生物学的产业化落地率先发生在国外,Ginkgo Bioworks、Lodo Therapeutics、Zymergen、Synlogic、Indigo Agriculture等创业公司已经成为合成生物技术领域的明星企业。其中,将合成生物技术和人工智能结合起来,应用于电子工业新材料开发的Zymergen,成长格外迅速。
2013年,Jed Dean和Zach Serber在美国加州埃默里维尔成立Zymergen。在此之前,他们在合成生物技术公司 Amyris 研发可再生能源。在尝试改造微生物去生产生物燃料的过程中,两人发现使用传统的研发方式进展缓慢——10个设计方案的测试需要1个月时间才能完成,他们希望运用自动化来加快实验进程,并把这种想法落地在Zymergen。
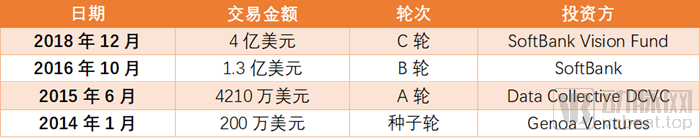
Zymergen将智能和自动化技术融入到设计、构建和测试的全流程中,并结合海量的?物组学数据,使得工程化改造微生物的效率成倍提升,并将其应用于柔性有机发光半导体(flexible OLED)等新型电子工业材料的开发。据Crunchbase记载,Zymergen成立近7年来,总共完成4轮超过5亿美元融资。
蓝晶微生物于2019年10月与央企化工巨头中化国际(600500.SH)在清华大学签署战略合作协议,双方共同推动生物基可降解材料PHA的产业化,是国内合成生物技术产业化的一项重要进展。
用生物实验的自动化构建技术壁垒
由于生物系统的复杂性,在活细胞内设计基因通路是一项难度极大的工作。蓝晶微生物研发团队的基因通路设计和开发能力在全世界处于领先地位,顾问团队更是合成生物技术领域一系列技术标准和理论的早期奠基者。具有生物与物理复合学术背景的张浩千博士曾在5年前设计并合成了包含>50个基因元件的基因通路,该通路的复杂度至今无人超越;李腾博士则凭借其将合成生物技术应用于工业微生物领域的成就在2019年入选《麻省理工科技评论》评选出的中国区“35位35岁以下科技创新青年”和《财富》杂志中国40位40岁以下商界人物。目前,蓝晶微生物已经建立起国内外产业界独有的基因通路设计平台,该平台面向医疗、环保和消费领域的分子和材料创新需求可辐射千亿美元规模的全球市场。

蓝晶微生物工作流(资料来源:蓝晶微生物)
在张浩千博士看来,阻碍合成生物学进一步发展的因素主要有两个:
第一,每碱基对DNA的合成成本限制了合成生物技术所能处理的生物系统的规模。尽管在过去20年中,DNA合成成本已经降低1000倍,但至少还需要一个数量级的成本降低,才能在任意生物细胞中开展基因组规模的工程化改造。
第二,生物实验自动化的程度决定了设计、构建和测试的循环迭代速度。高通量、良好集成的自动化实验将大大加快数据采集的过程,拓宽数据记录和分析的维度,提高生物研发结果的再现性。
蓝晶微生物正在构建一个依靠自动化技术研发细胞工厂的流水线,并逐步使用智能来取代传统解读实验数据,公司自主开发的Holog系统能够存储、分析所有的实验过程数据。
李腾博士表示,“现阶段,我们研发自动化平台的聚焦点是测试环节,这对于蓝晶微生物进行高效率的微生物定制开发非常关键。”