瑞德西韦(remdesivir)在中国的临床试验已暂停。
昨日,根据ClinicalTrials.gov网站显示,瑞德西韦在中国进行的用于治疗轻度至中度COVID-19成人患者的试验的注册状态显示为“已暂停”,其原因是中国COVID-19流行已得到控制,无法招募符合要求的入组患者。
上周末,针对重症COVID-19患者的临床试验也由于入组率低被暂停。
这项研究执行严格的随机双盲试验,以评价瑞德西韦在新冠状病毒性肺炎的疗效和安全性。也就是说,患者与医生都不清楚所服用的究竟是试验药还是安慰剂,一定要等到揭盲时才能确信药物效果。
该研究于2020年2月启动,预计4月27日完成,但目前来看,瑞德西韦在中国的研究将无法继续进行。
瑞德西韦目前尚未在全球任何国家获得批准,对于治疗新型冠状病毒肺炎的安全性或有效性尚不明确。
但此前在世界各地新增的试验将继续进行,其中一项已公布试验结果。
4月10日,《新英格兰医学杂志》(NEJM) 发表了一篇关于在研药物瑞德西韦对少数重症新型冠状病毒肺炎患者的治疗结果分析,首批53名新型冠状病毒患者获得瑞德西韦同情用药后,68%的病情得到缓解。
吉利德方面称,这些患者是无法参加临床试验的危重患者,通过同情用药程序,他们接受了瑞德西韦的治疗。这53名患者的早期数据并非通过临床试验获得,且数据只覆盖了少数接受瑞德西韦治疗的危重患者。
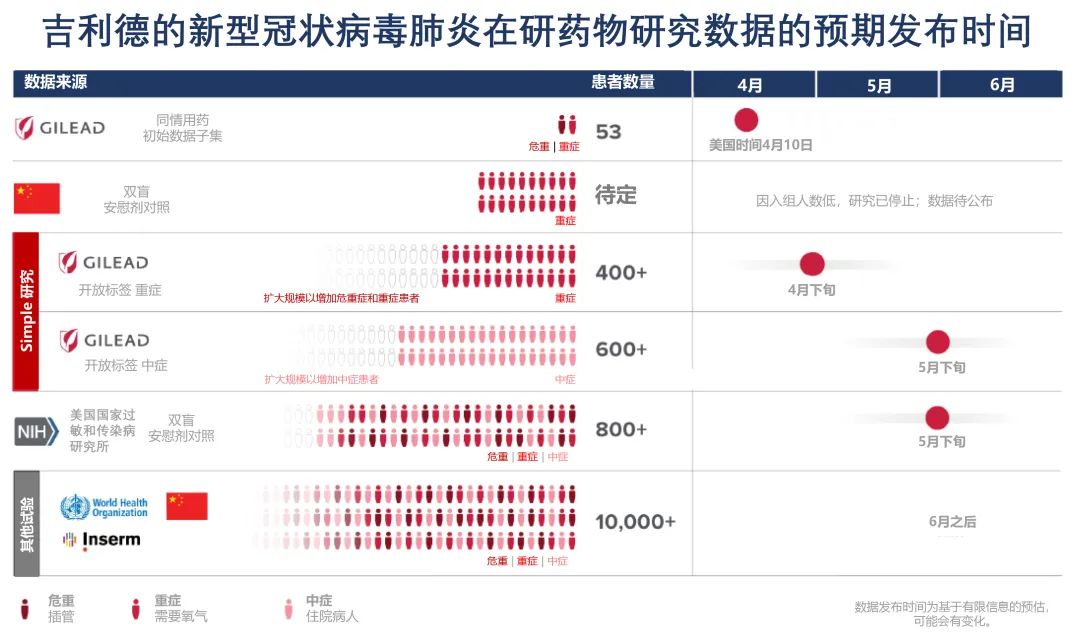
此外,吉利德正在美国、亚洲和欧洲的新型冠状病毒肺炎高发地区进行两项三期研究。其中一项研究针对重症患者,另一项研究针对中症患者。吉利德表示,这些研究要回答的众多问题之一是治疗时间是否可以从10天缩短到5天。重症的入组患者人数已达到了最初设计要求的人数,他们现在已经扩大了研究范围,让包括接受机械通气的患者在内的更多患者可以参与其中。
美国国家过敏和传染病研究所(NIAID)于2月21日开始了一项全球试验。该试验将随机分配患者使用瑞德西韦或安慰剂,以对照比较试验结果。该试验正在入组约800名具有不同症状的患者。
世界卫生组织也在进行一项全球试验,名为Solidarity,Inserm DisCoVeRy试验最近已在欧洲开始。
吉利德预计,4月底,他们将获得瑞德西韦针对重症患者研究的初步数据,并会迅速进行数据解读并分享结果。5月,他们将获得有安慰剂对照的NIAID试验的初步数据,以及吉利德的针对中度症状新型冠状病毒肺炎患者的研究数据。




